Inició ensayos clínicos el primer candidato vacunal cubano específico contra la COVID-19 (+ Fotos y Video)

La Habana, 24 de agosto de 2020. Tal como se había previsto y anunciado, Soberana, el primer candidato vacunal cubano específico contra la COVID-19 bajo la categoría de FR (Front Runner), e identificado por las siglas FINLAY-FR-1, inició su fase I de ensayos clínicos.
El sitio clínico escogido es el Centro Nacional de Toxicología (Cenatox), donde se administró el producto a los primeros 20 voluntarios seleccionados, en el rango etario de 19-59 años, cumpliendo todos los protocolos de buenas prácticas para este tipo de estudios, refirió a Cubadebate, la doctora Meiby de la Caridad Rodríguez González, directora de investigaciones clínicas del Instituto Finlay de Vacunas.
“El Cenatox fue escogido como la unidad de ensayos clínicos y es la responsable de velar por las buenas prácticas clínicas, de tal manera que la seguridad de los sujetos se encuentre a buen resguardo y que los datos sean confiables, trazables, reproducibles de modo que sea este estudio transparente y auditable por las autoridades competentes”, explicó el doctor Carlos Alberto González Delgado, jefe de la Unidad de ensayos clínicos del Cenatox.
De acuerdo con la información publicada en el Registro Público Cubano de Ensayos Clínicos, el estudio, nombrado Soberana 01, será aleatorizado, controlado, adaptativo y multicéntrico y tiene el propósito de evaluar la seguridad, reactogenicidad e inmunogenicidad del candidato en un esquema de dos dosis.
La muestra incluirá a 676 personas de entre 19 y 80 años, sin alteraciones clínicamente significativas y que otorguen por escrito su consentimiento informado de participación en el estudio. En cada intervención se conformarán dos grupos etarios, uno de 19–59 años y otro de 60–80 años.
Para la primera etapa del ensayo se espera que la administración de la vacuna sea segura, con no más de 5% de individuos con eventos adversos graves. En una segunda etapa se desea que la proporción de sujetos con respuesta inmune sea superior en al menos 50% con respecto al grupo de control.
Según el Registro Público Cubano de Ensayos Clínicos, el estudio debe concluir el 11 de enero y los resultados estar disponibles el 1ro. de febrero de 2021, para ser publicados el 15 de febrero.
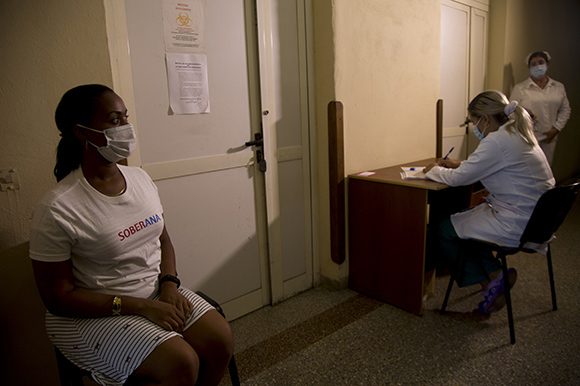
Inician fase I de ensayo clínico del candidato vacunal cubano Soberana.
Foto: Ismael Francisco/ Cubadebate.

Diana Carla Borges, 22 años, una de los primeros 20 voluntarios. Foto: Ismael Francisco/ Cubadebate.

Equipo del Centro Nacional Coordinador de Ensayos Clínicos (Cencec) encargado de la conducción y vigilancia del progreso del ensayo. Foto: Ismael Francisco/ Cubadebate.

Inician aplicación del candidato vacunal cubano Soberana. Foto: Ismael Francisco/ Cubadebate.
(Cubadebate, Video de YouTube)



