[:es]Donde se ensaya la esperanza [:]
[:es] Una noticia se hizo eco en los medios de comunicación cubanos y extranjeros cuando en 1996, con la estreptoquinasa recombinante (Heberkinasa), uno de los primeros productos insignia de la biotecnología cubana, el país logró reducir en un 33 por ciento la tasa de mortalidad intrahospitalaria por infarto agudo del miocardio.
Una noticia se hizo eco en los medios de comunicación cubanos y extranjeros cuando en 1996, con la estreptoquinasa recombinante (Heberkinasa), uno de los primeros productos insignia de la biotecnología cubana, el país logró reducir en un 33 por ciento la tasa de mortalidad intrahospitalaria por infarto agudo del miocardio.
Entonces se habló del Centro de Ingeniería Genética y Biotecnología (CIGB), promotor del fármaco que permitió, además, incorporar una terapéutica novedosa para el tratamiento de esta afección, que se ha mantenido en la práctica médica y se encuentra hoy extendida a la atención primaria.
También se mencionó por aquella fecha al Centro Nacional Coordinador de Ensayos Clínicos (Cencec), la institución surgida solo cinco años antes —en noviembre de 1991— y que permitió la inclusión de 2 915 pacientes de todas las provincias del país y del Municipio Especial Isla de la Juventud en el ensayo clínico del fármaco, un hecho y una cifra sin precedentes en Cuba.
A más de 20 años de finalizado este estudio, el de mayor número de pacientes incluidos desarrollado por el Cencec durante sus 26 años de existencia, En Red te propone un acercamiento a su participación directa en el desarrollo biotecnológico cubano y a la importante labor que realizan sus especialistas en el diseño, conducción y control de ensayos clínicos en el país.
El Centro, que tiene su sede en la capitalina calle 5ta. A entre 60 y 62, Miramar, Playa, cumple entre sus múltiples funciones con la confección de protocolos de investigación, la selección de sitios e investigadores, la elaboración de estrategias para el alistamiento de pacientes, el monitoreo de los ensayos clínicos, la realización de auditorías, el manejo y procesamiento de datos, la elaboración de informes finales, la capacitación de investigadores y la preparación de sitios para inspecciones y certificación por la autoridad reguladora.
Y no es que sean los únicos, sino que, si bien muchas empresas de la industria biotecnológica cubana cuentan con especialistas y equipos de trabajo capacitados para estos procesos, su especialización, repercusión en el registro sanitario e influencia directa en el sistema de salud cubano, avalan el prestigio que ya alcanza dentro y fuera del territorio nacional.
El arte de la experiencia
Cuando en 1981, solo cinco años después de la fundación en Estados Unidos de la primera industria biotecnológica del planeta, el Comandante en Jefe Fidel Castro inauguró la pionera de este tipo en el país, estaba consciente del potencial humano de la Isla y de que en poco tiempo la ciencia cubana comenzaría a dar los frutos que demandaban el desarrollo nacional y el sistema sanitario impulsado por la Revolución desde sus primeros instantes.
Así surgieron centros promotores del sector como el CIGB y el Centro de Inmunología Molecular (CIM), por solo mencionar dos de los más conocidos, pero también otros enfocados al conocimiento necesario para guiar las investigaciones que estos necesitaban con el objetivo de evaluar sus productos de investigación con el Cencec.
Según el máster en Ciencias Carlos Manuel García García, director de la entidad desde 2016, el desarrollo del polo científico a inicios de la década de 1990, la creciente producción de la industria cubana y la existencia de instituciones similares en todo el mundo, motivaron la creación de esta institución, que hoy goza de reconocimiento internacional.
Ensayos clínicos terminados por el Cencec según el centro promotor (1992-2016)
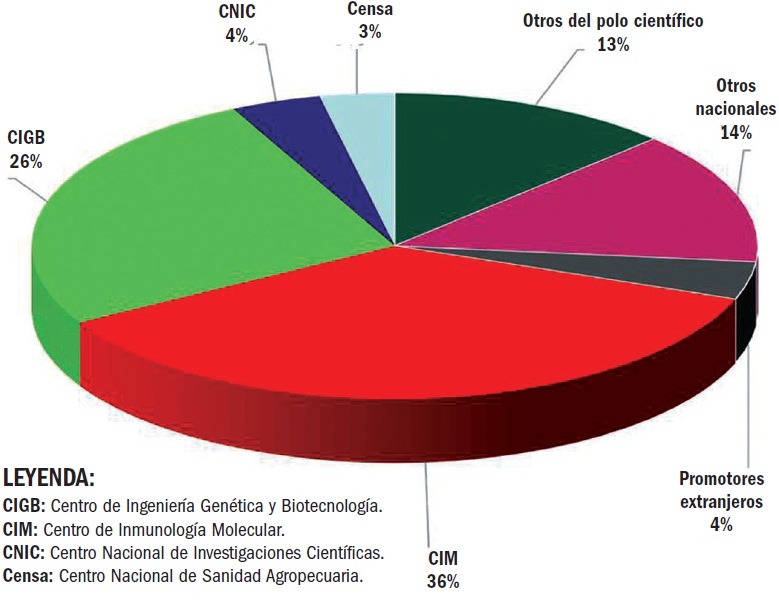
Solo para tener una idea de la importancia que posee, explicó, al cierre de 2016 el centro había concluido 150 ensayos clínicos de 28 centros promotores (ver gráfico 1) con 59 productos, y la participación de 1 245 sitios clínicos, 6 006 investigadores y 20 825 pacientes en pos de la evaluación clínica de nuevos productos por la entidad reguladora cubana —el Centro para el Control Estatal de Medicamentos, Equipos y Dispositivos Médicos de la República de Cuba (Cecmed)—, con la que comparten edificación desde el 14 de julio de 2014.
De estos 150 ensayos, según la máster en Ciencias Mayté Amoroto Roig, subdirectora a cargo de los ensayos clínicos en la institución, la mayoría (103) se corresponde con productos biotecnológicos y biológicos. Además, hay 22 productos farmacéuticos, 14 naturales, seis equipos, cuatro biomateriales y un diagnosticador.
Dentro de los estudios desarrollados predominan las especialidades de oncología (41), dermatología (13), gastroenterología (12), hematología (11), neurología (seis), angiología y cirugía vascular (seis), caumatología (cinco), cardiología (cuatro), inmunología (cuatro), estomatología (cuatro), angiología (cuatro), así como otras especialidades quirúrgicas (tres) y clínicas (37).

De izquierda a derecha, los másteres en Ciencias Mayté Amoroto Roig, Carlos Manuel García García y Gladys Jiménez Rivero. Foto: Laura Borges Moreno
Entre los 59 productos que ayudaron a evaluar desde su fundación y que hoy constituyen insignias dentro de la industria biotecnológica cubana, la directiva mencionó al interferón alfa recombinante (IFN alfa 2b), producido por el CIGB y cuyo uso fue evaluado en las indicaciones de la papilomatosis respiratoria — infección de garganta causada por un virus del papiloma humano (HPV)—, asociada a la cirugía en niños y adultos, la hepatitis crónica C en niños y adultos, la hepatitis C crónica y aguda, la leucemia mieloide crónica, el mieloma múltiple, la esclerosis múltiple y la esquizofrenia paranoide.
«El estudio fase IV de este fármaco tributó igualmente a que se constituyera un programa nacional de extensión terapéutica que incluyó a la totalidad de los pacientes (adultos y niños) con esta enfermedad en el país, y logró reducir la frecuencia de recaídas de los papilomas», dijo.
La inmunoglobulina antihepatitis B y su uso profiláctico en recién nacidos de madres portadoras de antígeno de superficie de este virus, fue otra de las que tuvo un gran impacto, sobre todo en el control de ese tipo de pacientes desde el punto de vista epidemiológico.
«Las características del estudio, extendido a todas las maternidades del país, permitió no solo el registro del producto, sino su introducción en la casi totalidad del territorio nacional y un incremento hasta el 99 por ciento de la cobertura de protección que brinda la vacuna contra la hepatitis B», explicó.
Promovido por el Centro Nacional de Sanidad Agropecuaria (Censa), el Surfacén y su uso en el distress respiratorio por membrana hialina del recién nacido —insuficiencia en la producción del surfactante pulmonar y falta de desarrollo pulmonar—, también fue estudiado y validado por los especialistas del Cencec. Los resultados del estudio clínico desarrollado facilitaron la introducción y extensión controlada de esta terapéutica en la casi totalidad de los servicios de neonatología del país, y la reducción del 0,2 por ciento de la tasa de mortalidad infantil por esta afección.
Destacada participación ha tenido el Cencec en la evaluación de los productos del CIM y el registro de importantes productos para la atención médica de pacientes con diversas tipologías de cáncer, como el Nimotuzumab en el cáncer de cabeza y cuello y de cerebro, y el Racotumomab y el CimaVax en el cáncer del pulmón. Este último se extendió a la atención primaria de la salud con la participación de alrededor de 160 policlínicos y 25 instituciones hospitalarias, permitiendo que los pacientes puedan recibir el tratamiento próximo a su área de residencia.
Se destaca también el diagnosticador de embarazo (Heberfastline), evaluado en varias instituciones del país gracias a la labor del Cencec, que permitió la adopción de este producto por el sistema de salud cubano reduciendo las importaciones de dispositivos con esa función.
El Centro también participó en la evaluación del Heberprot-P, producto registrado en Cuba y otros países para el tratamiento de la úlcera del pie diabético.
Prioridad al conocimiento
Conducir un ensayo clínico ya sea desde sus instantes iniciales o en determinados momentos no resulta una tarea sencilla, ni puede ser realizado por una sola persona, asegura la máster en Ciencias Mayté Amoroto Roig, a cargo de esta actividad desde 2015.
Lo principal, asegura, es la preparación del equipo de investigación, desde el investigador líder hasta todo el personal que participa en el ensayo, así como los miembros del Comité de Ética de la Investigación, sin los cuales sería imposible la evaluación de los productos de la biotecnología cubana. De ahí la importancia que le atribuyen en la entidad a la formación y superación profesional de todos sus especialistas, e incluso de quienes desde los centros promotores acuden al Cencec en busca de orientación o preparación para encaminar sus ensayos.
En los últimos tiempos, aseguró, hemos tenido un mayor número de ensayos multicéntricos y mayor solicitud de asesoramiento y orientación durante las fases previas al registro sanitario, por lo que cada día debemos superarnos para brindarle a cada cliente el servicio que necesitan con la mejor calidad posible. Solo así garantizamos una más pronta evaluación e incorporación al mercado nacional de los productos de la biotecnología que tanto demanda nuestro pueblo.
Esta ha sido siempre una de las premisas de la entidad, que luego de trabajar durante el pasado año en 42 ensayos clínicos con seis promotores, 20 productos, 435 sitios clínicos, 3 215 investigadores clínicos, 258 pacientes incluidos y 2 045 pacientes en seguimiento; y recibir solicitudes de compañías farmacéuticas internacionales para realizar investigaciones conjuntas, se prepara para afrontar en 2018 lleno de nuevos proyectos que tributen igualmente a este objetivo.
Así lo aseguró el también doctor Carlos García García, directivo de la entidad, al tiempo que anunció la participación actual del centro en varios proyectos de ensayos clínicos con el Instituto Finlay, entre los que sobresalen una vacuna contra el neumococo y otra contra el cólera. Asimismo, dijo, su equipo de trabajo está dispuesto a participar en todos los nuevos proyectos de investigación que a nivel nacional e internacional utilicen la biotecnología en beneficio de la salud y el bienestar de las personas.
Como retos de cara al futuro más inmediato, mencionó, se suma a los presentados por el Ministerio de Salud Pública de garantizar la estabilidad epidemiológica del país (se trabaja en 17 ensayos clínicos vinculados a este objetivo); disminuir la mortalidad materna e infantil (20 ensayos clínicos); reforzar el registro de los comités de ética en las instituciones de salud pública no solo para garantizar una mayor transparencia y seguridad de los estudios que allí se realicen, sino también para ofrecerles cada día una mejor atención a los pacientes; continuar trabajando en el enfoque salubrista del sistema de salud cubano; e incrementar la apertura de los servicios que brinda hacia el exterior.
La transparencia de un registro vital
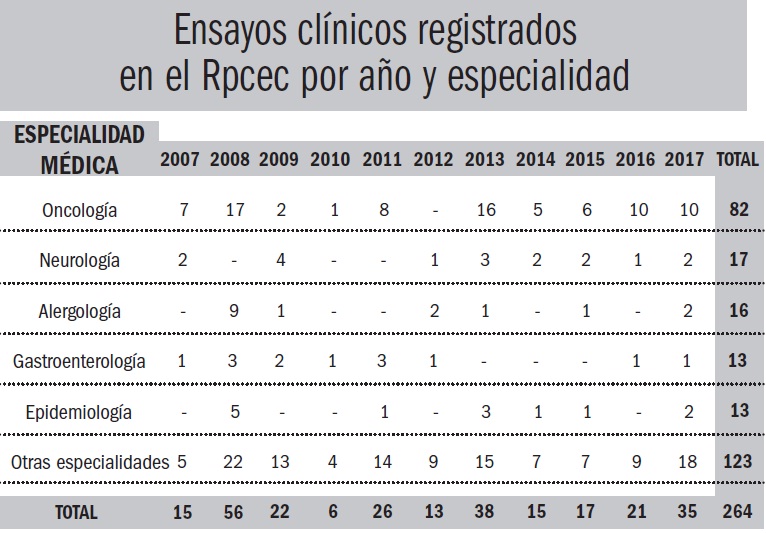
Entre los logros que exhibe el Cencec sobresale el Registro público cubano de ensayos clínicos (Rpcec), creado en junio de 2007 por especialistas de la entidad y que hasta el 4 de enero de este año agrupaba a un total de 264 ensayos.
Sobre esta importante herramienta la máster en Ciencias de la Computación y ensayos clínicos Gladys Jiménez Rivero, jefa del departamento de manejo y procesamiento de datos y responsable del Rpcec, explicó que, con la publicación de sus datos tanto en idioma español como en inglés, persigue ser una de las tantas fuentes de información sobre todos los ensayos clínicos que se realizan en el país, no necesariamente coordinados por el Cencec.
Disponible para todos los interesados nacionales y extranjeros a través de la dirección electrónica www.rpcec.sld.cu o como enlace dentro del sitio web del Centro, el repositorio, que surgió como una herramienta para hacer más transparente todo el proceso que acompaña a los ensayos clínicos en Cuba, forma parte de la red de registros internacionales de la Organización Mundial de la Salud desde 2011.
Según explicó la especialista, hasta este momento los interesados en conocer de alguno de estos estudios pueden encontrar allí la información básica de presentación de cada ensayo, y a partir de un proyecto en el que se trabaja desde 2007 pretenden comenzar este año a incluir el reporte resumido de los resultados de cada ensayo registrado.
(Tomado de Juventud Rebelde)[:]




